En fusionnant avec le laboratoire de biologie médicale de l’Institut Pasteur en 1999, le Laboratoire Cerba a acquis des compétences étendues dans le domaine des maladies infectieuses.
En sa qualité de laboratoire de référence en France, le Laboratoire Cerba est à la pointe de la surveillance épidémiologique.
Le périmètre mondial de son activité lui permet d’être particulièrement informé des variations régionales des génotypes viraux, fournissant ainsi une connaissance précise et parfaitement à jour de la diffusion des virus et des stratégies thérapeutiques optimales.
En employant et en collaborant avec des spécialistes de renommée mondiale, le Laboratoire Cerba est capable de réagir très rapidement aux nouvelles menaces infectieuses et de développer de nouveaux tests dans un temps très court pour offrir aux cliniciens, aux patients et aux autorités de santé des opportunités de diagnostic fiables et rapides.
Les arbovirus, ces virus transmis par des arthropodes (moustiques, tiques, phlébotomes) sont responsables de maladies le plus souvent asymptomatiques ou modérées et spontanément résolutives, mais parfois invalidantes (Chikungunya) voire sévères (Dengue hémorragique, Encéphalite West-Nile ou TBE, Syndromes de Guillain –Barré post Zika) ou potentiellement dangereuses pour la femme enceinte (Zika).
La présence de vecteurs potentiels de ces arbovirus et en particulier d’Aedes albopictus dans certains départements métropolitains rend possible le démarrage d’une épidémie autochtone pendant la période estivale. Aussi le diagnostic et la surveillance des cas d’arboviroses sont-ils particulièrement importants, aussi bien dans les régions d’endémie outre-mer qu’en métropole pour les cas d’importation, surtout pendant la période « à risque » de mai à novembre.
Le diagnostic repose sur la détection d’antigènes ou d’acides nucléiques viraux par PCR dans la phase aigüe de la maladie, et secondairement sur la sérologie IgG et IgM.
Le Laboratoire Cerba est en mesure de proposer le diagnostic direct et/ou sérologique de plusieurs arboviroses qui sévissent dans différentes régions du monde : les virus de la Dengue et du Chikungunya dans pratiquement toutes les régions tropicales, le virus Zika actuellement en amérique du sud et aux antilles mais aussi en Afrique , en Asie et dans le Pacifique, le virus West-Nile dans le pourtour méditerrannéen et en Amérique du Nord, le virus TBE (encéphalite à tiques) dans l’est de la France et dans toute l’europe centrale et de l’est.
Infection par le virus Zika :
Le virus Zika (ZIKV) est un arbovirus à ARN de la famille des Flaviviridae, proche des virus de la Dengue. Il a été isolé pour la première fois chez le singe en Ouganda en 1947. Il est transmis par les moustiques de la famille des Aedes, dont Aedes albopictus, vecteur également de la Dengue et de Chikungunya. Deux lignées, africaine et asiatique, ont été décrites comme responsables avant 2007 de cas sporadiques et de petites épidémies chez l’homme en Afrique et en Asie. Une première émergence épidémique de la souche asiatique en Micronésie en 2007 a été suivie d’une épidémie en Polynésie Française en 2013 puis en Nouvelle Calédonie en 2014. En mai 2015 la présence du virus Zika a été confirmée au Brésil comme responsable d’une épidémie de syndromes éruptifs fébriles débutée en février dans le Nord-Est du pays. Depuis cette date le virus a atteint la majorité des pays d’Amérique du sud, d’Amérique centrale et des Antilles, dont les départements français d’Amérique, et l’archipel du Cap-Vert. L’épidémie est considérée comme terminée aux Antilles depuis la fin 2016 mais des cas sporadiques restent décrits. Par ailleurs le virus circule toujours en Asie du sud-est et dans plusieurs archipels du Pacifique.
Il est responsable chez l’homme d’infection aiguës, majoritairement asymptomatiques. Les manifestations cliniques observées sont modérées, difficiles à différencier de la Dengue et de Chikungunya, associant fièvre, myalgies et arthralgies, céphalées, possibles conjonctivites et/ou éruptions maculo-papuleuses. La maladie est spontanément résolutive en quelques jours, sans séquelles. Les formes sévères sont très rares.
Cependant une augmentation significative de l’incidence de syndromes de Guillain–Barré a été décrite en Polynésie comme au Brésil, et une augmentation significative du nombre de naissances d’enfants atteints de microcéphalie a été décrite dès octobre 2015 au Brésil, superposable dans le temps et dans l’espace à l’épidémie de Zika. La Polynésie française avait également rapporté une augmentation du nombre d’anomalies du développement cérébral in utero contemporaine de l’épidémie de Zika dans l’archipel. La responsabilité directe du virus a depuis été confirmée.
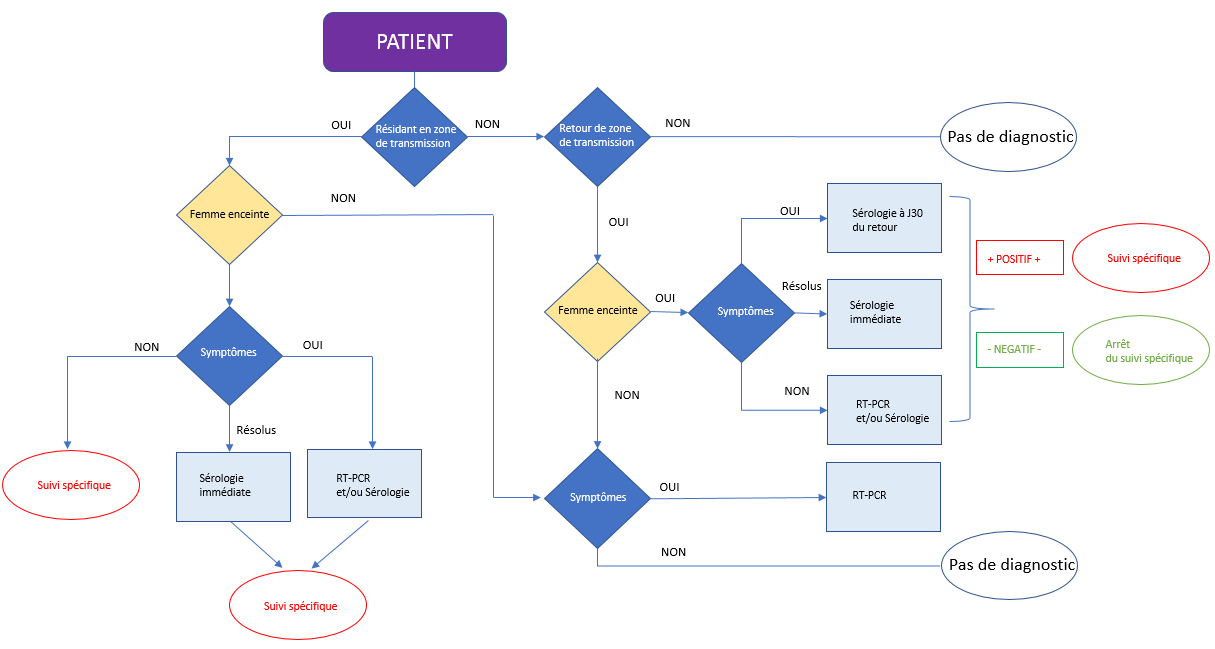
Le diagnostic de l’infection repose essentiellement sur la détection de l’ARN viral par RT-PCR en temps réel dans le plasma ou le sérum au tout début de la maladie (< 5 jours) en raison d’une virémie très courte. L’ARN viral peut aussi être détecté dans les urines pendant 10 à 15 jours après le début des signes cliniques.
La sérologie (IgM puis IgG) se positive au bout d’environ une semaine. Les réactions sérologiques croisées avec les autres Flaviviridae, en particulier la Dengue, sont possibles en IgG. Par ailleurs la sensibilité des tests IgM est faible, rendant le diagnostic sérologique délicat d’interprétation.
Un point sur le virus Zika
Surveillance des infections humaines par Hantavirus en France métropolitaine, 2012-2016
 Les infections par les Hantavirus chez l’homme font l’objet d’une surveillance en France, en particulier en métropole, depuis une trentaine d’années. Cette surveillance associait sur la période 2012-2016 un réseau d’une quinzaine de laboratoires de biologie médicale, le Centre national de référence (CNR) des Hantavirus et Santé publique France. Les données de surveillance ont été obtenues par l’analyse des fiches de renseignements accompagnant les échantillons des cas diagnostiqués par les laboratoires du réseau et confirmés par le CNR.
Les infections par les Hantavirus chez l’homme font l’objet d’une surveillance en France, en particulier en métropole, depuis une trentaine d’années. Cette surveillance associait sur la période 2012-2016 un réseau d’une quinzaine de laboratoires de biologie médicale, le Centre national de référence (CNR) des Hantavirus et Santé publique France. Les données de surveillance ont été obtenues par l’analyse des fiches de renseignements accompagnant les échantillons des cas diagnostiqués par les laboratoires du réseau et confirmés par le CNR.
La situation observée était proche de celles rapportées pour les périodes précédentes : une centaine de cas, la plupart hospitalisés, était dénombrée en moyenne annuellement (incidence de 0,15 cas pour 100 000 habitants) avec de fortes variations annuelles. La population active était toujours la plus touchée (médiane d’âge de 40 ans) et les hommes étaient les plus concernés (75% des cas). Les cas étaient détectés toute l’année, avec des pics de détection a la fin du printemps ou a l’automne. La majorité des cas étaient dus au virus Puumala, mais le fait marquant sur la période était la détection de cas d’infection par les virus Seoul et Tula et la nature des expositions à ces virus. La distribution géographique des cas, concentrée sur le quart nord-est de la France, a connu une extension très limitée dans sa périphérie. Cependant, cette incidence et cette distribution géographique pourraient être sous-estimées du fait de l’utilisation de tests de diagnostic sérologique trop spécifiques et de la faible demande de diagnostic pour des patients non hospitalisés ou en dehors de la zone d’endémie connue.
L’hiver marque la recrudescence des infections respiratoires aiguës. Ces pathologies, d’étiologie souvent virale, sont d’évolution spontanément favorable dans la population générale. Cependant, aux âges extrêmes de la vie, chez le sujet immunodéprimé, en cas de pathologie respiratoire sous jacente, la prise en charge du malade peut se compliquer avec le recours possible à une hospitalisation.
Récemment de nouvelles techniques de biologie moléculaire sont apparues permettant la détection simultanée d’agents pathogènes des voies respiratoires. Grace à ces techniques, l’identification précise du ou des pathogènes associés aux pneumopathies communautaires est passée de 40% à plus de 70%. Sont identifiés des virus : Virus Grippal A et B, Parainfluenzavirus, Virus Respiratoire Syncytial, Métapneumovirus, Adénovirus, Entérovirus, Rhinovirus, Bocavirus, Coronavirus et des bactéries : Legionella pneumophila, Mycoplasma pneumoniae et Chlamydia pneumoniae.
Le bénéfice associé à la connaissance du pathogène responsable réside dans : l’instauration éventuelle d’un traitement antiviral adapté, la réduction du recours à une antibiothérapie, la mise en œuvre de mesures d’isolement du malade adaptées et la réduction de la durée d’hospitalisation.
Le test est réalisé à partir d’un écouvillonnage ou d’une aspiration nasopharyngé, le résultat est rendu dans la journée.
Détection moleculaire d'agents pathogènes des voies respiratoires
Retrouvez toutes les actualités